Prediksi Soal Ujian Nasional Kimia SMA Tahun 2018
Squad, Ujian Nasional SMA 2018 hanya tinggal lima hari lagi, lho. Bagaimana kabarmu di masa-masa menjelang ujian ini? Mungkin kamu merasa takut, khawatir, atau harap-harap cemas dalam menghadapi Ujian Nasional yang sudah di depan mata ini. Nah, tidak perlu panik lagi, sekarang kita akan belajar tentang prediksi soal UN Kimia SMA 2018. Soal seperti apa ya yang kira-kira akan muncul nanti? Yuk, kita pelajari!

1. Topik : Perkembangan teori atom
Teori atom yang mengatakan bahwa elektron beredar mengelilingi inti pada orbit tertentu adalah model atom….
- Dalton
- Thomson
- Rutherford
- Niels bohr
- mekanika kuantum
Jawaban : D
Pembahasan :
Perkembangan teori atom terdiri dari :
- Teori atom Dalton menyatakan bahwa atom merupakan bola pejal yang tidak bisa dibagi – bagi lagi
- Teori atom Thomson menyatakan bahwa di dalam atom terdapat elektron yang tersebar secara merata. Model ini sering disebut dengan model atom roti kismis.
- Teori atom Rutherford menyatakan bahwa massa atom terpusat pada inti atom yang bermuatan positif dan sebagian besar volume atom merupakan ruangan hampa (tidak bermuatan)
- Teori atom Niels Bohr menyatakan bahwa elektron dalam atom beredar mengelilingi inti atom pada lintasan energi tertentu yang disebut kulit atom
- Teori atom mekanika kuantum terdiri dari teori Schrodinger, de Broglie dan Heissenberg. Teori atom ini menjelaskan mengenai kebolehjadian penentuan letak elektron yang tidak dapat dijelaskan oleh teori atom Bohr.

2. Topik : Menghitung pH asam – basa![]() adalah ….
adalah ….
- 2 – log 2
- 2
- 2 + log 2
- 12
- 12 + log 2
Jawaban : E
Pembahasan :
![]() merupakan basa kuat bervalensi 2. Penentuan pH basa kuat adalah sebagai berikut :
merupakan basa kuat bervalensi 2. Penentuan pH basa kuat adalah sebagai berikut :
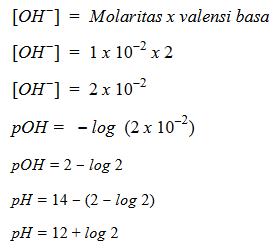

3. Topik : Titrasi berdasarkan grafik
Perhatikan grafik berikut!
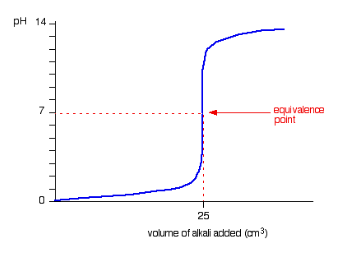
Kurva titrasi di atas dihasilkan dari titrasi….
- asam kuat – basa kuat
- basa kuat – asam kuat
- asam kuat – basa lemah
- basa kuat – asam lemah
- asam lemah – basa lemah
Jawaban : A
Pembahasan :
Jika dilihat dari grafik, titik awal titrasi dimulai dari angka pH yang mendekati 0, maka dapat disimpulkan bahwa sebelum dititrasi, zat yang ada merupakan asam kuat. Sedangkan titik akhir titrasi mendekati nilai pH 14, maka setelah titrasi, terdapat spesi basa kuat. Sehingga kurva titrasi tersebut terbentuk dari titrasi asam kuat oleh basa kuat. Asam kuat disebut titran dan basa kuat disebut (pentiter). Hal ini diperkuat oleh titik ekuivalen yang tercapai yaitu pada pH = 7, artinya ketika jumlah mol asam = mol basa, larutan bersifat netral. Hal ini hanya terjadi pada titrasi asam kuat oleh basa kuat.

4. Topik : Endapan Ksp
Jika diketahui nilai Ksp AgCl = ![]() , maka pencampuran 100 ml
, maka pencampuran 100 ml ![]() 0.01M dengan 100 ml KCl 0.001M akan akan menghasilkan….
0.01M dengan 100 ml KCl 0.001M akan akan menghasilkan….
- larutan tepat jenuh
- larutan belum jenuh
- endapan KCl
- endapan AgCl
- larutan terlarut sempurna
Jawaban : D
Pembahasan :
Untuk memprediksi hasil dari pencampuran 2 larutan, maka diperlukan nilai Qsp.
Qsp < Ksp → campuran larut sempurna (belum jenuh)
Qsp = Ksp → campuran tepat jenuh
Qsp > Ksp → campuran membentuk endapan (lewat jenuh)
Penentuan nilai Qsp adalah sebagai berikut:
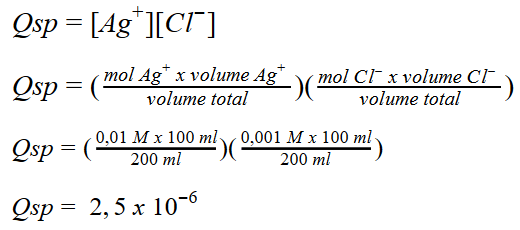
Karena Qsp > Ksp maka akan terbentuk endapan AgCl.

5. Topik : Perubahan entalpi
Jika diketahui nilai ![]() senyawa adalah sebagai berikut:
senyawa adalah sebagai berikut:
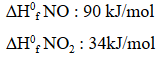
Maka nilai perubahan entalpi pembakaran 60 gram gas NO (Mr = 30) adalah….
- -112 kJ
- – 56 kJ
- -23 kJ
- + 56 kJ
- + 112 kJ
Jawaban: A
Pembahasan:
Persamaan reaksi pembakaran gas NO adalah sebagai berikut:
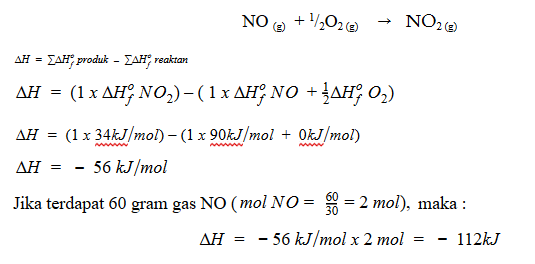

6. Topik : Variabel bebas dan terikat laju reaksi
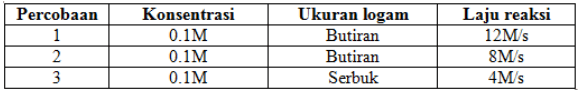
Berdasarkan data tersebut, variabel bebas, variabel terikat, dan variabel terkontrol berturut – turut adalah….
- konsentrasi – ukuran logam – laju reaksi
- laju reaksi – ukuran logam – konsentrasi
- konsentrasi – laju reaksi – ukuran logam
- ukuran logam – laju reaksi – konsentrasi
- laju reaksi – konsentrasi – ukuran logam
Jawaban : D
Pembahasan :
Variabel bebas adalah variabel yang diubah – ubah untuk menentukan pengaruhnya terhadap variabel terikat, yaitu ukuran logam. Variabel terikat adalah variabel yang diukur, yaitu laju reaksi. Variabel terkontrol adalah variabel yang tidak berubah – ubah atau tetap, yaitu konsentrasi.

7. Topik : Pergeseran kesetimbangan
Perhatikan reaksi kesetimbangan berikut!
![]()
Jika suhu sistem dinaikkan, maka kesetimbangan akan….
- bergeser ke arah kanan
- bergeser ke arah kiri
- tidak terjadi pergeseran
- terjadi reaksi bolak – balik
- tidak dapat diketahui
Jawaban : A
Azas Le Chatelier menyatakan bahwa jika suatu sistem kesetimbangan dikenakan aksi, maka sistem tersebut akan melakukan reaksi untuk meminimalkan pengaruh aksi tersebut. Salah satu aksi yang dapat memengaruhi kesetimbangan adalah suhu. Jika suhu dinaikkan, maka sistem kesetimbangan akan bergeser ke arah endoterm yaitu ke arah ∆H positif. Sebaliknya, jika suhu diturunkan, maka kesetimbangan akan bergeser ke arah eksoterm (ke ∆H negatif). Nilai ∆H yang diketahui dalam suatu persamaan reaksi adalah untuk reaksi ke kanan. Sehingga pada reaksi di atas, jika suhu dinaikkan, kesetimbangan akan bergeser ke arah kanan (endoterm).

8. Topik : Hukum Faraday
Dalam proses elektrolisis, sejumlah arus listrik yang sama dialirkan melalui larutan ![]() dan larutan
dan larutan ![]() yang disusun dalam rangkaian seri. Jika 0,635 gram Cu mengendap, maka massa logam Cr yang mengendap sebanyak…. (Ar. Cu = 63,5 Ar. Cr = 52)
yang disusun dalam rangkaian seri. Jika 0,635 gram Cu mengendap, maka massa logam Cr yang mengendap sebanyak…. (Ar. Cu = 63,5 Ar. Cr = 52)
- 0.17 gram
- 0.35 gram
- 0.42 gram
- 1.12 gram
- 2.0 gram
Jawaban : B
Pembahasan :
Reaksi yang terjadi adalah sebagai berikut :
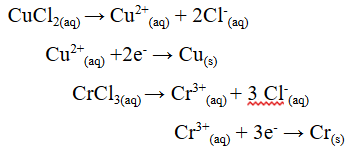
Berdasarkan Hukum Faraday II, penentuan massa logam yang terendapkan dalam rangkaian seri proses elektrolisis adalah sebagai berikut:
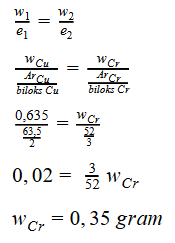

9. Topik : Tata nama senyawa
Jika larutan amonium sulfat direaksikan dengan larutan kalium hidroksida akan menghasilkan gas amonia, larutan kalsium sulfat dan air. Rumus senyawa amonium sulfat adalah….
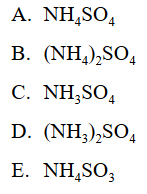
Jawaban : B
Pembahasan:
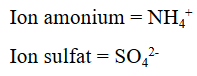
Untuk membentuk senyawa netral amonium sulfat, maka 2 ion amonium akan bereaksi dengan 1 ion sulfat sesuai persamaan reaksi sebagai berikut :
![]() Sehingga rumus senyawa amonium sulfat adalah
Sehingga rumus senyawa amonium sulfat adalah ![]()

10. Topik : Hukum dasar kimia
Pada reaksi antara gas hidrogen dan gas oksigen dihasilkan sejumlah uap air. Apabila gas hidrogen yang direaksikan sebanyak 12 liter, maka gas oksigen yang diperlukan dan uap air yang dihasilkan sebanyak….
- 24 liter – 12 liter
- 12 liter – 6 liter
- 6 liter – 12 liter
- 12 liter – 24 liter
- 24 liter – 6 liter
Jawaban : C
Pembahasan:
Persamaan reaksi antara gas Hidrogen dan gas Oksigen adalah sebagai berikut :
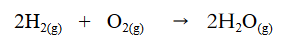 Berdasarkan hukum Gay Lussac, dinyatakan bahwa perbandingan volume gas – gas yang bereaksi sebanding dengan koefisien gas tersebut. Maka, jika direaksikan 12 L gas Hidrogen, jumlah gas Oksigen yang diperlukan sebanyak 6 L dan uap air yang dihasilkan sebanyak 12 L.
Berdasarkan hukum Gay Lussac, dinyatakan bahwa perbandingan volume gas – gas yang bereaksi sebanding dengan koefisien gas tersebut. Maka, jika direaksikan 12 L gas Hidrogen, jumlah gas Oksigen yang diperlukan sebanyak 6 L dan uap air yang dihasilkan sebanyak 12 L.
Itulah tadi sepuluh soal prediksi Ujian Nasional Kimia SMA 2018. Semoga dapat membantu kamu dalam mengerjakan ujian nanti ya, Squad. Jika masih belum paham dan merasa membutuhkan bantuan, kamu bisa langsung mencari guru privat sesuai kriteriamu di ruangles. Selamat menempuh Ujian Nasional 2018!












