Mengetahui Cara Menentukan Rumus Molekul Senyawa

Squad, sebelumnya kamu sudah mengetahui cara menentukan rumus empiris senyawa ‘kan? Selanjutnya kita bahas cara menentukan rumus molekul senyawa, yuk! Rumus molekul merupakan kelipatan-kelipatan dari rumus empiris. Lalu, bagaimana cara menentukan rumus molekul senyawa? Kita simak penjelasan di bawah ini yuk, Squad!
Rumus molekul menyatakan jenis dan jumlah atom yang sebenarnya di dalam molekul suatu senyawa. Rumus molekul dapat diartikan sebagai kelipatan dari rumus empirisnya. Untuk menyatakan rumus molekul suatu zat dilakukan dengan cara menuliskan lambang kimia tiap unsur yang ada dalam molekul dan jumlah atom dituliskan di kanan lambang kimia unsur secara subscript contohnya glukosa mempunyai rumus molekul C6H12O6, yaitu setiap molekul glukosa mengandung enam atom karbon (C), dua belas atom hidrogen (H), dan enam atom oksigen (O).

Glukosa memiliki rumus molekul C6H12O6 (Sumber: kabarpenting.com)
Cara mengetahui rumus molekul senyawa dari rumus empiris yaitu harus diketahui terlebih dahulu massa molekul relatifnya. Rumus molekul dan rumus empiris senyawa hanya terjadi perbedaan jumlah atom, sedangkan atom unsur penyusun senyawa tetap. Namun demikian beberapa senyawa memiliki rumus molekul dan rumus empirisnya yang sama, misalnya H2O (air) dan NH3 (amoniak).
Supaya kamu lebih paham, coba kerjakan contoh soal di bawah ini ya

Diketahui:
m = 4,2 gram
T = 435 K
P = 1 atm
V = 2,5 liter
Ditanya: Rumus molekul?
Jawab:
Asumsikan gas senyawa bersifat ideal maka jumlah mol uap dicari menggunakan persamaan gas ideal, yaitu:
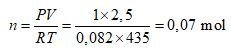
Setelah jumlah mol diketahui, selanjutnya menentukan massa molekul relatif senyawa (Mr) yang dapat dihitung melalui massa molar, nilai massa molar juga menyatakan nilai massa molekul relatif dari senyawa.
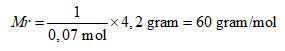
Dengan demikian massa molekul relatif adalah 60 sma.
Massa molekul relatif merupakan kelipatan dari massa rumus empiris. Dari rumus empiris, diketahui senyawa tersusun dari saru atom C, dua atom H dan satu atom O. Dengan demikian:
Mr = n x (Ar C + 2 Ar H + Ar O)
60 = n x (12 + 2 + 16)
60 = n x 30
n = 2
dengan n = 2, rumus molekul senyawa tersebut adalah:
2 x (CH2O) = C2H4O2
Jadi, rumus molekul senyawa adalah C2H4O2. Berdasarkan rumus molekul dan sifat-sifat senyawa diketahui bahwa senyawa tersebut adalah asam asetat.
Oke Squad, sekarang kamu sudah tahu kan cara menentukan rumus molekul senyawa? Rumus molekul ini bisa dicari dari rumus empiris asalkan diketahui massa molekul relatifnya. Kalau kamu masih punya pertanyaan lain tentang materi ini, langsung saja tanyakan melalui ruanglesonline. Kamu tinggal foto pertanyaan kamu dan tutormu akan langsung menjawabnya lho Squad. Gunakan sekarang, kuy!













